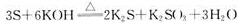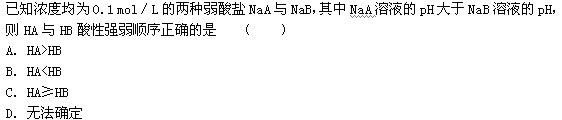2010年成人高考高起点《化学》命题预测试卷(2)
-
第 31 题常温常压下将20.0 g 14.0%的NaCl溶液,和30.0 g 24.0%的NaCl溶液混合,得到密度为1.15g/cm3的混合溶液,试计算:
(1)该混合液的质量分数。
(2)该混合液的物质的量浓度。
-
第 29 题将0.65 g锌全部溶于200 mL稀盐酸中,然后加入80 mL 0.5 mol/L AgNO3溶液,恰好使Cl-离子沉淀完全。试计算:
(1)产生多少升(标准状况下)氢气。
(2)原稀盐酸的物质的量浓度为多少。
-
第 30 题

-
第 28 题IA族中某金属元素的单质19.5g跟足量的盐酸反应,生成氢气5.6 L(标准状况),该元素的相对原子质量是__________。
-
欲使某物质的不饱和溶液变成饱和溶液,可采用的方法有__________、__________或__________。
-
第 24 题钢铁的电化学腐蚀中,有析氢腐蚀和吸氧腐蚀两种形式,写出吸氧腐蚀中正极反应的化学方程式:__________ 。
-
第 25 题如图所示是一套实验室制气装置,用于发生、干燥和收集气体,下列各组物质中能利用这套装置讲行实验的是__________(填序号)。
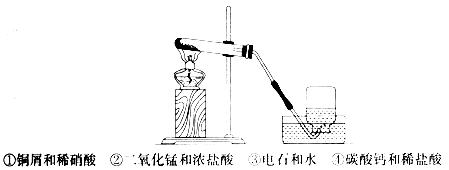
-
第 26 题已知A+B==C+D,20g A与15gB恰好完全反应生成10g C,则B与D的摩尔质量比是__________。
-
第 22 题25.在加热条件下,硫跟氢氧化钾溶液反应的化学方程式为:
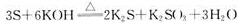
在此反应中,被氧化和被还原的物质的物质的量之比为__________。
-
第 23 题某烃的分子量为128,试写出该烃可能的两种分子式:__________、__________。
-
第 20 题氯水中存在如下平衡 。向氯水中加入少量CaCO3,平衡向反应方向移动,向氯水中加入少量饱和食盐水,平衡向--反应方向移动(填“正”或“逆”)。
-
第 21 题为了防止FeCl2变质,可以加入一定量的__________或__________。
-
第19题写出下列化学反应的离子方程式。
(1)明矾在水中产生能吸附其中悬浮杂质的物质:__________。
(2)Mg在NH4Cl溶液中能产生H2的原因:__________。
-
第18题比较均为0.1 mol/L的①H2S溶液、②NaHS溶液、③Na2S溶液中c(S2-)大小:__________ (按由大到小的顺序填序号)。
-
第17题在实验室内制取CO2、NH3、H2、C2H2、Cl2、C2H4 6种气体时,能用如图所示的装置置制取的气体是__________。
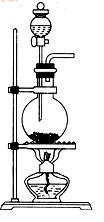
-
第 15 题
-
第16题某学生在做实验时,除去某物质中含有的杂质,所选用的试剂(括号内为所选试剂)错误的是__________(填序号)。
①苯中含有苯酚(浓溴水) ②乙酸乙酯中混有乙酸(乙醇)
③二氧化碳中混有SO2(小苏打) ④氯化铁中混有氯化铜(铁粉)
⑤乙炔中混有水蒸气(无水氯化钙)
-
第 14 题

-
第 13 题

-
第 12 题

-
第 10 题

-
第 11 题

-
第 8 题

-
第 9 题

-
第 7 题

-
第 5 题

-
第 6 题

-
第 4 题

-
第 3 题

-
第 1 题

-
第 2 题