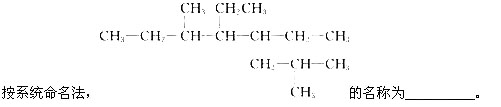第 21 题在1~18号元素中,电子总数是最外层电子数二倍的元素是__________,最外层电子数是次外层电子数二倍的是__________,次外层电子数是最外层电子数二倍的是__________。
-
第 31 题将0.56g铁粉加到50mL的1 mol/L盐酸溶液中,充分反应后,试计算:
(1)在标准状况下,可生成氢气多少升?
(2)假定反应后溶液的体积仍为50 mL,则溶液中的Fe2+和H+的物质的量浓度各为多少?
-
第 29 题将5.9g NaCl和NaBr的混合物溶于水后通人足量的Cl2使之充分反应,再将反应后溶液加热蒸干灼烧,得到残渣质量4.0g。计算原混合物中NaCl、NaBr的质量。
-
往50 mL稀硫酸和稀盐酸的混合溶液中加入2.1375 g氢氧化钡粉末,充分反应后进行过滤,测得滤液的pH=13,其沉淀干燥后质量为1.165 g。试计算原混合溶液中SO42-和Cl-的物质的量浓度。
-
第 27 题某未知溶液可能含有K+、Al3+、Fe2+、 、Cl-、S2-中的几种,为确定其组成,进行如下实验:
根据上述实验事实判断:溶液中肯定存在的离子有__________。
-
第 28 题有相同物质的量浓度的A、B、C三种一元酸的溶液,已知:
(1)A溶液的pH大于B溶液;
(2)B的钠盐溶液的碱性大于同浓度的C的钠盐溶液。
则这三种酸的酸性由强到弱的顺序是__________。
-
第 25 题已知某元素的气态氢化物为H2X,则它的最高价氧化物对应的水化物的通式为__________。若在氢化物中,氢与X的质量比为1:16,则X最高价氧化物对应的水化物的分子式为__________。
-
第 26 题已知0.1 mol R2O3的质量为16g,则R的相对原子质量为__________。
-
第 24 题将pH=3的硫酸溶液和pH=10的氢氧化钠溶液相混合,若要使混合溶液pH=7,则硫酸溶液和氢氧化钠溶液的体积比为__________。
-
第 22 题
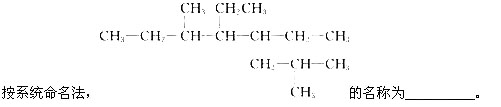
-
第 23 题

2005年初级经济师考试《旅游经济专
初级旅游经济师试题及答案一
初级旅游经济师试题及答案二
2005年初级经济师考试《邮电经济专
初级经济师试题及答案1(邮电经济)
初级经济师试题及答案1(保险经济)
初级经济师试题及答案2(邮电经济)
初级经济师试题及答案2(保险经济)
初级经济师试题及答案3(保险经济)
2014年经济师初级考试真题《建筑经