某初中化学教师在一次测验中设计了下列试题,并对部分学生的解题结果进行了统计和分析。
【试题】实验室现有3瓶失去标签的无色溶液。已知它们分别是NaNO3、NaCl、Na2CO3的溶液,请设计实验方案,将他们一一鉴别。
【考试结果】有30%的学生提交了下面的方案:分别取三种溶液样品少量,放入三支试管中,向三支试管各滴入稀盐酸,有气泡冒出的溶液是Na2CO3溶液,再向无明显现象的两支试管里分别滴AgNO3溶液,有白色沉淀产生的原溶液是NaCl溶液,无明显现象的原溶液是NaNO3溶液。根据上述信息,回答:
(1)请设计出本实验正确的鉴别方案。
(2)试对上述学生答题错误的原因进行分析。
(3)写出本实验中涉及的有关化学反应方程式。
-
阅读材料,根据要求完成教学设计任务。
材料一 《义务教育化学课程标准(2011年版)》关于“酸和碱的中和反应”的内容标准为:“认识常见酸碱的主要性质和用途”;活动与探究建议:“设计实验证明氢氧化钠与盐酸能发生化学反应”
材料二 教科书的内容结构体系
第十单元 酸和碱
课题1 常见的酸和碱
课题2 酸和碱的中和反应
材料三 教科书“酸和碱的中和反应”所呈现的内容
课题2 酸和碱的中和反应
一、中和反应
酸有相似的化学性质,碱也有相似的化学性质。那么,酸与碱能否发生反应呢?
实验10-8如图10-13所示,在烧杯中加入约5mL稀氢氧化钠溶液,滴入几滴酚酞溶液用滴管慢慢滴入稀盐酸,并不断搅拌溶液,至溶液颜色恰好变成无色为止。
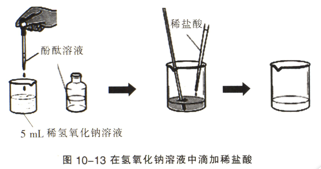
可以发现,上述反应中生成的氯化钠、氯化钙和硫酸钠都是由金属离子和酸根离子构成的,我们把这样的化合物叫作盐。盐在水溶液中能解离出金属离子和酸根离子。
酸与碱作用生成盐和水的反应,叫作中和反应。
材料四 学校条件和学生发展现状符合一般要求。
要求:
(1)设计“三维”教学目标。
(2)确定教学重点和难点。
(3)设计教学过程(包括新课导入、展示、总结)。
(4)设计教学板书。
-
某初中化学教师在一次测验中设计了下列试题,并对部分学生的解题结果进行了统计和分析。
【试题】实验室现有3瓶失去标签的无色溶液。已知它们分别是NaNO3、NaCl、Na2CO3的溶液,请设计实验方案,将他们一一鉴别。
【考试结果】有30%的学生提交了下面的方案:分别取三种溶液样品少量,放入三支试管中,向三支试管各滴入稀盐酸,有气泡冒出的溶液是Na2CO3溶液,再向无明显现象的两支试管里分别滴AgNO3溶液,有白色沉淀产生的原溶液是NaCl溶液,无明显现象的原溶液是NaNO3溶液。根据上述信息,回答:
(1)请设计出本实验正确的鉴别方案。
(2)试对上述学生答题错误的原因进行分析。
(3)写出本实验中涉及的有关化学反应方程式。
-
阅读下列材料,回答有关问题:
素材1
公元前5世纪,安培多克勒提出四种原质说,认为世界皆由水、火、气、土4种原质构成。在公元前4世纪,四原质说为亚里士多德所发展,他在四原质的基础上提出四原性:冷、热、干、湿。冷与干则是土,冷与湿则是水,热与干则是火,热与湿则是气。由于四元论具有感官表象的一致性,亚里士多德的四元论能为人们广泛接受,并统治人们长达2000多年。
素材2
1784年左右,卡文迪许研究了空气的组成,发现空气中氮气的体积占4/5,氧气占1/5。此外,他还确定了水的成分,从而肯定了空气是混合物而不是元素,水是化合物而不是元素。
1789年,拉瓦锡在《化学概述论》中明确提出了元素的操作定义:用现有的化学分析手段都无法分解的物质,可姑且称为“元素”。按照这样的定义,化学家们渐渐意识到早在人们学会利用火进行化学分析的时候,就已经能分解出11种单质:铜、铁、金、锡、银……
1800年,戴维对伏打电堆做了改进,发现很多在火的作用下不分解的物质却经不起电的作用1807~1808年,戴维用电化学方法分解出钠、钾、钡、钙、镁、锶6种活泼金属,使分解某些活泼的金属化合物得以实现。1814~1817年,约瑟夫·冯·夫琅禾费制造了一个棱镜光谱仪,可以观察到600多条暗线一本生和基尔霍夫证明,根据两谱线在光谱中的位置可以得知某种特定金属的存在,利用这种方法都可以检测到含量极少的金属元素。
素材3
1803年英国化学家道尔顿提出原子论后,受到科学界的普遍重视,原子论的核心是:每种元素以其原子的质量为其最基本的特征、因此,测定原子量的工作成为当时化学的重点工作道尔顿和贝采里乌斯分别以氢和氧为基准,对原子的质量进行了测量。1869年,人们已经发现了63种元素,门捷列夫按原子量的大小和元素的化学性质之间的关系列成一张表,这便是他的第一张元素周期表门捷列夫的假说跟以往假说相比具有三个优势:一是对当时测不准的9种元素的原子量做了必要的修正;二是根据原子量的增长是有规律的这一科学假设,给周期表预留了6个空位;三是从当时的原子量测定数据来看,碲比碘重,钴比镍重,门捷列夫根据这两对元素的性质,将它们的位置做了必要的调整。
根据上述材料,简要同答问题:
(1)从元素周期表的发现始末,归纳出科学的化学理论发展需要经过哪些阶段。
(2)从上述材料概括出影响化学科学发展的因素有哪些。
(3)恩格斯说“门捷列夫不自觉地应用黑格尔的量转化为质的规律,完成了科学上的一个勋业。”你如何理解这句话。
-
案例:
对于学生探究实验“质量守恒定律的探究”,难点不是实验操作,而是怎样通过实验认识质量守恒定律。
[教材处理]
将教材中的三个实验分成六个组来做:1、2两个组做“氢氧化钠溶液和硫酸铜溶液反应”的实验;3、4组做“碳酸钠粉末和盐酸反应”的实验;5、6组做“硫酸铜溶液和铁片反应”的实验。
[过程设计]
环节一:分组实验,发现差异
环节二:回顾反思,探究原因
环节三:汇报交流,得出结论
[现场记录]
当1、2、5、6四个小组的实验结果符合质量守恒定律,而3、4组做的实验与质量守恒定律不符时,同学们展开了讨论。
学生甲:我们组发现在方案三中有气体生成了,产生的气体逸到空气中去,使得我们无法测量他们的重量。
学生乙:我们通过联系以前的知识得知,化学反应的实质就是分子破裂,原子重新组合成新的分子的过程,从这里我们得知原子的种类、数量、性质在化学变化中并没有发生变化,既然反应前后原子没有发生变化,反应前后原子的总质量也应该没有发生变化,所以我们确定化学反应中反应物的质量等于生成物的质量。
问题:
(1)上述案例中教师利用了哪些教学资源?
(2)上述案例中教师引导学生采用了哪些学习方式?
(3)上述案例中,该教师在教学设计、教学实施两方面的做法体现了哪些课程理念?
-
MgCl2、KCl和MgSO4等物质的溶解度曲线如下图所示。下列说法正确的是( )。
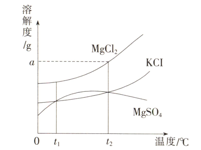
- A.MgSO4的溶解度始终随温度的升高而减小
- B.t1℃时,KCl和MgSO4两溶液所含溶质的质量一定相等
- C.t2℃时,100 g MgCl2的饱和溶液中含有a g MgCl2
- D.将t1℃时的KCl饱和溶液升温到t2℃,溶液由饱和变为不饱和
-
W、X、Y、Z四种短周期元素在周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知()。

- A.X元素形成的单核阴离子还原性大于Y
- B.Z元素氧化物对应水化物的酸性一定强于Y的
- C.X、Y、Z中最简单氢化物稳定性最弱的是Y
- D.Z元素单质在化学反应中只表现氧化性
-
某化学教科书在呈现新知识之前,通过“活动探究”“资料”等栏目及图片学习情景的设计,引导学生对身边的自然和社会环境的联想,驱动学生探究的动机,明确探究的任务和意义,这种设计主要运用了()。
- A.认识结构教学理论
- B..多元智能理论
- C..最优教学理论
- D..先行组织者理论
-
设NA为阿伏伽德罗常数的值,下列有关叙述正确的是()。
- A.标准状况下,2.24 L H2O含有的氧原子数为0.1NA
- B.常温下,14 g N2中的氮原子数为0.5NA
- C.2 L 0.5mol/L亚硫酸溶液中含有的氢离子数为2NA
- D.23 g Na在空气中充分燃烧时,转移电子数为NA
-
化学学习过程中,学生按照自己对知识的理解,用结构网络的形式表示出概念的意义以及与其他概念之间联系的学习策略是()。
- A.概念形成策略
- B.概念同化策略
- C.问题解决策略
- D.概念图策略
-
下列递变规律正确的是( )。
- A.NH3、SiH4、HF的热稳定性依次增强
- B.LiOH、NaOH、CsOH溶液的碱性依次增强
- C.O、S、Na的原子半径依次增大,而离子半径依次减小
- D.HCl、HBr、HI的还原性依次增强,其水溶液的酸性依次减弱
四川省2001年会计从业资格考试《会
2008年会计从业资格考试会计实务模
2004年上海上半年会计从业资格考试
2010年会计职称初级会计实务全真模
2010年会计职称初级会计实务全真模
2010年会计职称初级会计实务全真模
2010年会计职称初级会计实务全真模
2010年会计职称初级会计实务全真模
江苏2010年《初级会计电算化》考试
2010年湖南会计从业考试《初级会计


